
Non-CF-Bronchiektasen
Lorem ipsum dolor sit amet, consetetur sadipscing elitr, sed diam nonumy eirmod tempor invidunt ut labore et dolore magna aliquyam erat, sed diam voluptua. At vero eos et accusam.
Nicht durch eine zystische Fibrose (cystic fibrosis, CF) bedingte Bronchiektasen (Non-CF-Bronchiektasen) …
- stellen einen heterogenen Erkrankungskomplex mit vielen zugrundliegenden Ursachen und dementsprechend häufig eine diagnostische und therapeutische Herausforderung dar,
- sind gekennzeichnet durch eine dauerhafte Erweiterung der Bronchien und Bronchiolen und einem Teufelskreis aus chronischer Infektion und Entzündung, Sekretverhalt und Schädigung der Atemwege,
- gehen aufgrund der erheblichen klinischen Beschwerden und des chronisch-progredienten Verlaufs mit einer außerordentlichen Belastung und Einschränkung der Alltagsfähigkeit für die betroffenen Patienten einher.
Aufgrund eines eklatanten Mangels an epidemiologischen, grundlagen-wissenschaftlichen und klinischen Studien zu Non-CF-Bronchiektasen ist die Datenlage für die meisten angewandten Therapien dürftig. Dies kommt vor allem darin zum Ausdruck, dass auch 2018 noch keine zugelassene pharmakologische Therapie für diese Indikation existiert und notwendige Verordnungen abseits ihrer eigentlichen Zulassung („off-label“) erfolgen müssen.
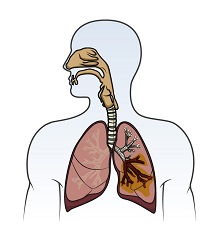
Was sind Bronchiektasen?
Bronchiektasen, bei denen als Ursache eine zystische Fibrose (CF) ausgeschlossen wurde, bezeichnet man als Non-CF-Bronchiektasen. Die Therapiekonzepte zur Lösung von Sekret und Verhinderung von Infektionen orientieren sich weitgehend an der Therapie der Mukoviszidose, anti-obstruktive Behandlungsschemata werden von der Therapie der COPD abgeleitet.
Als Bronchiektasen bezeichnet man eine permanente Dilatation von Bronchien und Bronchiolen als Folge einer Zerstörung der Muskulatur und des elastischen Bindegewebes. Am häufigsten beginnt die Erkrankung mit einer Einengung des Bronchialbaums durch eine Infektion, die bei einer Chronifizierung zu einer Zerstörung des Epithels führen kann. Die Störung der mukoziliären Clearance resultiert in einer Sekretretention, die für weitere Infektionen prädestiniert.
Früher entstanden Bronchiektasen meist post-infektiös infolge von Keuchhusten-, Masern- und Influenzaepidemien. Heute ist der postinfektiöse Weg die häufigste Ursache in den Entwicklungsländern. In den Industrienationen hat die Entwicklung von antibiotischen Therapien und Impfungen zu einer steten Abnahme der Erkrankungszahlen von Bronchiektasen bei Post-infektöser Ursache geführt. Aktuell sind mehr kongenitale als postinfektiöse Ursachen zu beobachten.
Ursachen
Verschiedenste Mechanismen können zur Entstehung von Bronchiektasen führen, die pathophysiologische Endstrecke ist jedoch gleich.
Zu Beginn steht meist eine Schädigung des bronchialen Epithels durch eine Entzündung, das umliegende Gewebe wird von Entzündungsszellen infiltriert. Die Zerstörung des benachbarten Gewebes führt zu einer Aussackung in Form von zylindrischen, varikösen und zystischen Ausweitungen mit Zerstörung der umgebenden Strukturen. Diese wiederum resultiert in einer defekten mukoziliären Clearance. Dadurch kommt es zu einer Sekretretention, die wiederum eine bakterielle Kolonisation mit chronischer Entzündung begünstigt. Weiter kommt es zu einer Verdickung der Bronchialschleimhaut, die histologisch deutliche Plattenepithelmetaplasien aufweist, ohne dass vermehrt Indizien für Malignome beobachtet werden.
Postinfektiös
Verschiedene respiratorische Infektionen können Bronchiektasen verursachen, dazu gehören:
> Pertussis
> Gramnegative Bakterien (Pseudomonas aeruginosa, Haemophilus influenzae)
> Viren (HIV, Paramyxovirus, Adenovirus und Influenza)
> Tuberkulose
> atypische Mykobakterien.
Angeborene Ursachen
Die häufigste angeborene Ursache für Non-CF-Bronchiektasen ist eine Primäre Ciliäre Dyskinesie (PCD). Ein unzureichender Zilienschlag führt zu einer verminderten Sekretclearance, diese hat eine erhöhte Infektrate zur Folge.
Eine weitere angeborene Ursache ist die Mutation im ENaC-Gen, die zu einem defekten epithelialen Natriumkanal führt. Ein hyperaktiver Natriumkanal bewirkt hierbei eine Störung der Salz- und Wasserhomöostase an der respiratorischen Schleimhaut.
Chronisch obstruktive Lungenerkrankung
30 – 50 % der Patienten mit fortgeschrittener chronisch obstruktiver Lungenerkankung (COPD) weisen Bronchiektasen auf. Diese Patienten leiden vermehrt unter Atemnot und haben eine schlechte Lungenfunktion. CT-morphologisch unterscheiden sich Bronchiektasen bei COPD von klassischen Bronchiektasen, da die Aussackungen selbst nicht so ausgeprägt ist, dafür jedoch eine ausgeprägte peribronchiale Infiltration besteht. Mit der steigenden Prävalenz der COPD weltweit kommt auch Bronchiektasen eine zunehmende Bedeutung zu.
Klinik
Patienten mit Bronchiektase klagen über chronischen Husten, Sputum-produktion und Lethargie. Husten mit blutigem Auswurf, Thoraxschmerz, Gewichtsverlust, Bronchospasmus, Atemnot und Leistungsminderung kommen ebenso vor. Das häufig erwähnte dreischichtige Sputum aus einer schaumigen Oberschicht, schleimigen Mittelschicht und zähem Bodensatz mit Eiter ist für die Erkrankung typisch, kommt jedoch nicht immer vor. Einige Patienten sind im Alltag symptomfrei und sind nur während einer Exazerbation klinisch auffällig.
Viele Patienten haben regelmäßige Exazerbationen, im Durchschnitt etwa 1,5 pro Jahr. Wenn mind. vier der folgenden Sympotome auftreten, spricht man von einer Exazerbation: Zunahme des Sputums mit Husten, vermehrte Atemnot, Fieber über 38 °C, verstärktes Giemen, Verschlechterung der Belastbarkeit, Müdigkeit, Verschlechterung der Lungenfunktion, radiologische Infektzeichen
Der Verlust der Lungenfunktion wird für Nichtraucher mit Bronchiektasen mit einem Anteil von circa 50 mL/Jahr angegeben. Faktoren, die für eine Progredienz der Erkrankung sprechen, sind häufige Exazerbationen, eine chronische Besiedlung mit Pseudomonas aeruginosa und der Nachweis einer systemischen Inflammation. Bei schwerer Bronchiektase kann es auch zu einer pulmonalen Hypertonie und zu einer systolischen und diastolischen Dysfunktion des linken Ventrikels kommen.
Diagnose
Eine mikrobiologische Untersuchung des Sputums gehört zur Standarddiagnostik bei Bronchiektasen. Beim Fortschreiten der Erkrankung mit wiederholten Exazerbationen und negativem Sputumbefund ist eine Bronchoskopie zur Materialgewinnung angezeigt.
Die Methode der Wahl ist die hochauflösende Computertomographie. Oft können Art und Lokalisation der radiologischen Veränderungen bereits Hinweise auf die Entstehung geben. Dabei sind Bronchiektasen in den proximalen Atemwegen typisch für eine allergisch bronchopulmonale Aspergillose, multiple noduläre Bronchiektasen können auf eine Infektion mit Mykobakterium-avium-Komplex hinweisen.
Therapie
Zur Behandlung von Bronchiektasen gibt es zahlreiche Therapiemöglichkeiten:
z.B. durch Ausgleich von fehlenden Immunglobulinen bei einem angeborenen Immundefekt
z.B. durch Inhalation 3-7%-iger Kochsalzlösung in Kombination mit täglicher Atemphysiotherapie / autogener Drainage, Rehabilitationsmaßnahmen
z.B. durch Impfungen gegen Grippe, Pneumokokken, Keuchhusten und Haemophilus influenzae Typ b und ggf. durch Antibiotika, auch in inhalativer Form bei chronischer Infektion durch den Problemkeim Pseudomonas aeruginosa
z.B. durch Inhalation bronchialerweiternder Medikamente (Betamimetika, bzw. Anticholinergika) entsprechend dem Ausmaß der Lungenfunktionseinschränkung
z.B. durch eine entzündungshemmende Therapie mit dem Makrolid-Antibiotikum Azithromycin
(Exazerbation), z.B. durch Antibiotika in Tablettenform oder als Infusion
Zusammenfassung
Durch verbesserte antibiotische Therapien und Impfprogramme sind mehr angeborene als postinfektiöse Ursachen für eine Bronchiektase zu beobachten. Verschiedene Mechanismen führen zu Bronchiektasen – die pathophysiologische Endstrecke aus Inflammation und Destruktion ist jedoch gleich.
Zur Diagnostik sollte eine Sputumprobe entnommen werden; beim Einsatz eines bildgebenden Verfahrens ist die hochauflösende Computertomographie die Methode der Wahl.
Die Therapie der Grundkrankheit sollte immer berücksichtigt werden. Die Basis der Behandlung beinhaltet Atem- und physiotherapeutische Maßnahmen. Die Therapie der Exazerbationen sollte entsprechend den Ergebnissen aus Erregerdiagnostik und Antibiogramm durchgeführt werden. Eine zusätzliche Gabe von inhalativen Antibiotika oder Makroliden muss im Einzelfall erwogen werden. Für lokal begrenzte Bronchiektasen stehen chirurgische Maßnahmen zur Verfügung.